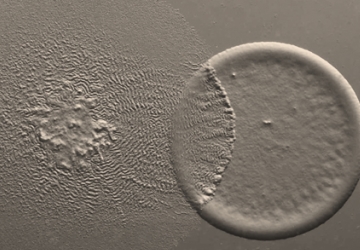
Myxococcus jagt im Schwarm
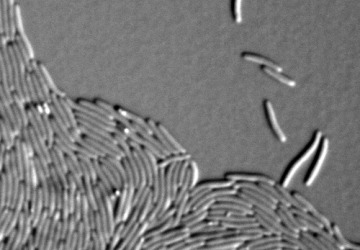
Sie rotten sich zu Hunderttausenden zusammen, belagern das Opfer und vernichten es schließlich: Myxococcus xanthus ist ein in der Gruppe aktiver Jäger, der andere Bakterien als Nahrungsquelle nutzt. Dazu müssen die winzigen stäbchenförmigen Bakterien miteinander kommunizieren und ihr Verhalten koordinieren. Dieses faszinierende und in sozialem Verband lebende Bakterium wählte die Vereinigung für Allgemeine und Angewandte Mikrobiologie (VAAM) zur Mikrobe des Jahres 2020.
Bei Nahrungsmangel lauert Myxococcus xanthus geschützt auf bessere Zeiten: Unzählige Zellen finden sich gezielt zu einem kugelförmigen Haufen zusammen und bilden einen Pilz-ähnlichen gelben Fruchtkörper. Die schlanken, stäbchenförmigen Zellen verwandeln sich in runde Sporen, die Hunger- und Trockenzeiten überdauern können. Fruchtkörper und Sporen verdankt das Bakterium seinen Namen: Die Fruchtkörper sind gelb (griech. xanthos), die Sporen kugelig (coccos), und die Zellen produzieren einen Schleim (myxa), der die Gemeinschaft zusammenhält. Der größte Teil hungernder Zellen löst sich jedoch auf und dient als Nahrungsquelle – kannibalistischer Selbstmord zum Überleben der Population. Ein kleiner Teil stäbchenförmiger Zellen bleibt außerhalb des Fruchtkörpers und hilft, neue Nahrungsquellen zu erkennen. Ist der unwirtliche Zustand vorüber, bilden sich aus den verbliebenen Stäbchen und Sporen des Fruchtkörpers wieder aktive Zellgemeinschaften, die erneut zum Beutezug ausschwärmen.
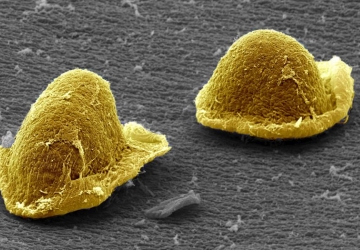
Faszinierende Sozialstrukturen
Der im Boden lebende Myxococcus xanthus ist ein Musterbeispiel für soziale Koordination unter einzelligen Mikroorganismen. Dafür ist eine präzise Kommunikation zwischen den Zellen notwendig. Verschiedene Signalstoffe und komplexe Empfangssysteme sorgen für eine Abstimmung benachbarter Zellen, wie sie selbst Mikrobiologen von ihren winzigen Forschungsobjekten kaum erwartet hatten. Der gemeinschaftlich gebildete Fruchtkörper ist fast mit bloßem Auge zu erkennen: Die Kugeln erreichen die Dicke eines Blatts Papier. Verwandte Myxobakterien bilden noch größere Bäumchen-ähnliche Strukturen von der Dicke eines Fingernagels.
Beweglich durch Ziehen und Gleiten
Die einzelnen Bakterien können sich auf zwei verschiedene Arten bewegen: Zum einen nutzen sie haarförmige Anhängsel (Pilus) aus tausenden Proteinuntereinheiten. Jeder einzelne Pilus kann sich verlängern, an Oberflächen anheften und dann wieder verkürzen. So entsteht eine Kraft, die die Zelle nach vorne zieht. Zum anderen können die Bakterien gleiten. Dabei heften sie sich mit Hilfe von Proteinkomplexen an den Untergrund. Diese Proteinkomplexe entstehen am vorderen Zellpol, binden an den Untergrund und wandern dann an das hintere Ende der Zelle. So schiebt sich die Zelle nach vorne. Beide Bewegungsmechanismen wiederholen sich kontinuierlich und bringen einzelne Zellen und große Zellgruppen koordiniert voran. „Es ist faszinierend, die unterschiedlichen Bewegungsmuster von M. xanthus in den räuberischen Schwärmkolonien und während der Fruchtkörperbildung zu beobachten“, so Myxobakterien-Forscherin Anke Treuner-Lange vom Marburger Max-Planck-Institut.
Baukasten für Medikamente
Kein Wunder, dass Myxococcus xanthus mit fast zehn Millionen Basenpaaren eins der größten bakteriellen Genome besitzt. Die aufwändige Lebensweise führt zudem dazu, dass Myxobakterien viele biologisch aktive Stoffe bilden, darunter Antibiotika zum Abtöten ihrer Opfer und Botenstoffe zur Kommunikation. Über 130 solcher Sekundärmetabolite (Stoffe, die nicht unmittelbar dem Stoffwechsel dienen) sind mittlerweile beschrieben.
Wie in einem Baukasten setzen die Myxobakterien verschiedene kleine Moleküle zu komplexen Stoffen zusammen. Dazu zählen beispielsweise die charakteristischen gelben Farbstoffe (DKxanthene), die eine wichtige Rolle bei der Entwicklung von Sporen zu aktiven Zellen spielen. Ein flüchtiger Stoff, Geosmin, ist für den typischen erdigen Geruch von M. xanthus verantwortlich.
Myxobakterien werden als Quelle für neue Antibiotika und Therapeutika zunehmend interessant. Das kürzlich entdeckte Corallopyronin könnte ein neues Breitbandantibiotikum werden. Der genetische Bauplan aus einem anderen Myxobakterium wurde in das Modellbakterium M. xanthus kloniert, um ausreichende Mengen an Corallopyronin herstellen und so die Wirksamkeit genauer untersuchen zu können.
Auf dem Weg zur Medikamentenentwicklung sind bereits antibiotisch wirkende Stoffe aus dem verwandten Myxobakterium Cystobacter. Diese Cystobactamide verhindern die korrekte Aufwicklung der bakteriellen DNA, wie sie für die Vervielfältigung nötig ist. Auch myxobakterielle Wirkstoffe gegen Krebs, Viren und im Pflanzenschutz gegen Pilzerkrankungen werden derzeit erforscht.
Weitere Informationen:

